「CRCはどんな書類を作成する?」の質問と回答のページです。質問に対しての回答投稿が可能です。マナーを守って有意義に利用しましょう。(削除申請はこちらからお願いします)
CRCはどんな書類を作成する?
 質問
質問

CRCはどんな書類を作成する?
CRCはたくさんの書類を作成するとWEBで読んだのですが、例えばどんな書類を作成するのでしょうか。いまいちイメージがわかなくて・・。詳しい方、教えてください! 2023年4月3日
2023年4月3日  5524
5524
 AIによる要約
AIによる要約
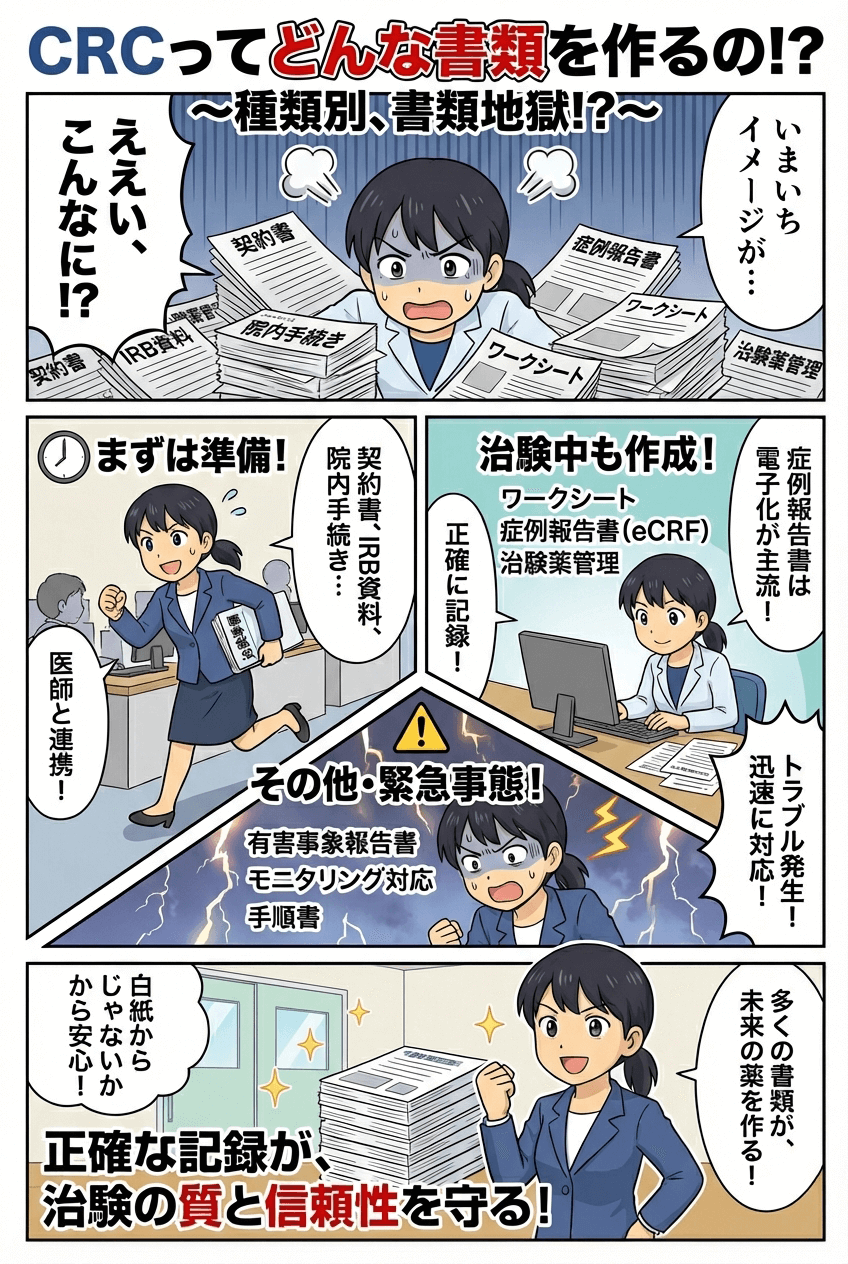
 マンガでわかる
マンガでわかる
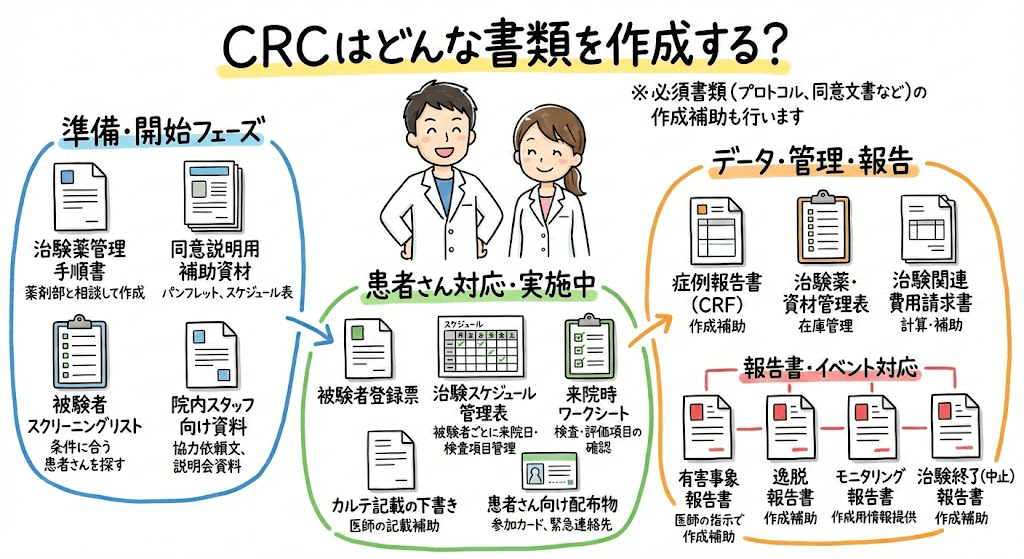
 イラスト・図解でわかる
イラスト・図解でわかる
 みんなの回答一覧
みんなの回答一覧
- CRCは、治験上必要な情報を集約するための様々の資料を作成します。 ベストアンサー
-
CRC3年目です。
CRCは、臨床試験の報告書(症例報告書)を最終的に作成するにあたり、患者の検査データや、副作用など、収集したデータを集約するための様々な書類があります。
---------
・調査票:製薬会社(依頼者)から試験の紹介があったとき、担当する施設に必要な検査機器があるか、候補者が何人いるかなどを事前に調査するシートです。
・スタートアップミーティング資料:医師やスタッフ向けに行う説明会で使う資料をCRCが補足するために作成することもあります。
・同意説明文書:依頼者から提供された同意説明文書を、施設の運用に則って記載整備を行います。
・統一書式:治験開始~終了まで使用する治験のフォーマット書式です。この書式に沿って治験審査委員会で報告します。主に医師が作成しますが、CRCが作成補助を行います。
・ワークシート:症例報告書を作成するため、各Visitで必要な検査を実施したか、検査値はいくつだったか、併用薬や有害事象はあったか等を取りまとめるシートです。
・原資料特定リスト:原データの所在を示すリストです。
・プロセスシート:治験がALCOAに従って行われていることを示すため、プロセスの全体像をまとめたシートです。
・精度管理/温度管理記録:検査機器が試験で求められている頻度で点検されているか、治験薬は決まった温度で保管されているかなどを記録するためのシートです。
---------
これでも上に挙げたものはほんの一部です(汗)。
治験は被験者の安全を守り、科学的な質を目指すため、対応した事柄は正確に記録へ残すことが求められます。なので、多くの書類が発生するんですね。ただ、統一書式や依頼者提供の書式があるため、白紙から作る書類はそれほど多くありませんので安心してくださいね。
 2023年4月23日
2023年4月23日
役に立った(4)
- 書類作成は欠かせない仕事です。 ベターアンサー
-
会社でも多少異なることはあるかと思いますが、被験者対応した後は「ワークシート」を作成します。内容はその被験者がいつ来院してどんな検査をしたか、どんな結果だったか等を記録する用紙です。医学的判断を伴う内容部分は医師に記載をお願いしに行きます。
また、被験者対応記録等、他のCRCに申し送り事項がある場合や次回被験者に確認が必要な事項等を書いておく用紙もあります。電話や口頭で被験者に伝えた内容を記録に残しておく場合もあります。
被験者対応以外にも治験費用を計算して請求書を作成したり、治験審査委員会に提出する書式の内容を作成することもあります。
トラブルが発生した場合に作成することが多い「逸脱に関する報告書」は医師が記載しますがCRCがサポートすることも多いです。
 2023年4月21日
2023年4月21日
役に立った(2)
- CRCが作成する書類
-
治験によって違いますが
ワークシート→他よりも全然多い
リスク管理シート
SAE報告書
ICF原案
請求書
などです
 2025年1月29日
2025年1月29日
役に立った(0)
- CRC(治験コーディネーター)が作成する主な書類 公式
-
CRC(治験コーディネーター)は毎日のように「ワークシート(チェックリストなど)」「症例報告書」「日報」を作成します。他にも、治験を新たに始めるときに「スタートアップミーティングに使う資料」、費用を請求するときには「請求書」を作成します。
また、統一書式(治験実施状況報告書、重篤な有害事象に関する報告書、逸脱に関する報告書、治験終了報告書)などもCRC(治験コーディネーター)が作成をサポートします。
以下のページも参考にしてください。
https://crc-bank.com/crcnoichinichi
(CRCの一日と一週間)
 2023年4月19日
2023年4月19日
- CRC(治験コーディネーター)が作成する書類について AI
-
CRCが作成する書類は、治験の種類や段階、実施医療機関の状況などによって異なりますが、大きく分けて以下の種類があります。
治験準備段階で作成する書類
◆ 治験依頼者との契約関連書類: 治験依頼者(製薬会社など)との間で取り交わす契約書や覚書など、治験実施に関する取り決めを記した書類の作成を補助します。
◆ 治験審査委員会(IRB)への提出書類: 治験実施の倫理性や科学性を審査するIRBに提出する書類の作成を補助します。具体的には、治験実施計画書(プロトコル)、同意説明文書、症例報告書の見本などが含まれます。
◆ 院内手続き関連書類: 治験を実施するために必要な院内手続き(例:倫理委員会への申請、院内各部署との調整など)に関する書類を作成します。
治験実施中に作成する書類
◆ 症例報告書(CRF): 治験に参加した被験者のデータ(例:病歴、検査結果、投与された薬剤、副作用など)を記録する重要な書類です。最近では、電子症例報告書(eCRF)が主流となっています。CRCは、カルテなどの原資料から必要なデータを収集し、CRFに正確に転記する作業を行います。
◆ 治験薬管理に関する書類: 治験薬の入荷、保管、払い出し、残薬管理などに関する記録を作成します。治験薬の管理状況を明確にするために重要な書類です。
◆ モニタリング報告書: 治験依頼者から派遣されたモニター(CRA)が実施するモニタリングの結果を記録する報告書の作成を補助します。モニタリングで指摘された事項への対応状況なども記録します。
◆ 有害事象報告書: 治験中に発生した有害事象(副作用など)を記録し、治験依頼者や規制当局に報告するための書類を作成します。
◆ 被験者対応に関する記録: 被験者への説明内容、同意取得状況、来院状況、問い合わせ内容などを記録します。
◆ その他、治験に関連する各種記録: 治験の進捗状況、関係者との連絡状況、その他治験に関連する事項を記録します。
治験終了後に作成する書類
◆ 治験総括報告書作成への協力: 治験の結果をまとめた総括報告書の作成に協力します。
その他の書類
上記以外にも、CRCは以下のような書類を作成する場合があります。
◆ 手順書・マニュアル: 治験の手順や方法をまとめた手順書やマニュアルを作成することがあります。
◆ 会議資料: 治験に関する会議(例:治験責任医師との打ち合わせ、院内関係者との会議など)で使用する資料を作成します。書類名 目的 内容 作成頻度 備考 治験実施計画書(プロトコル)関連 治験実施計画書(プロトコル)概要説明資料 治験の内容を医療機関スタッフに分かりやすく説明するため プロトコルの要約、治験の目的・方法、スケジュールなどをまとめた資料 治験開始時 治験責任医師と連携して作成 院内手順書 治験を円滑に進めるための院内ルールを定めるため 治験の流れ、各部署の役割分担、緊急時の対応などを記載 治験開始時、必要に応じて改訂 治験責任医師、院内関係者と協議して作成 被験者関連 同意説明文書 被験者に治験の内容を説明し、同意を得るため 治験の目的、方法、参加のメリット・デメリット、リスク、個人情報保護などを記載 治験開始前 治験依頼者(製薬会社)から提供された原案を基に、治験責任医師が施設に合わせて修正 同意書 被験者が治験参加に同意したことを証明するため 被験者の署名、日付、治験責任医師の署名などを記載 同意取得時 原本は医療機関で保管 服薬説明書 被験者に治験薬の服用方法を説明するため 服用量、服用時間、注意事項などを記載 治験薬交付時 治験薬管理者と連携して作成 服薬日誌 被験者が治験薬の服用状況を記録するため 服用日、時間、服用量などを記入する欄を設けた用紙 治験期間中 被験者に配布し、記入を依頼 症例報告書(CRF)関連 症例報告書(CRF) 治験データを治験依頼者(製薬会社)に報告するため 被験者の背景情報、治験期間中のデータ(検査結果、症状、有害事象など)を記載 データ取得後、適宜 現在は電子CRF(eCRF)が主流 原資料 CRFの根拠となる資料 カルテ、検査データ、問診票など データ取得時 CRFと照合するために保管 その他 モニタリング報告書 モニター(製薬会社の担当者)が医療機関を訪問した際の記録 訪問日、実施内容、指摘事項などを記載 モニタリング訪問後 モニターが作成する場合が多いが、CRCも内容を確認 治験薬管理記録 治験薬の入出庫、保管状況などを記録 治験薬のロット番号、数量、使用期限などを記載 治験期間中 治験薬管理者が作成 緊急時対応手順書 治験中に緊急事態が発生した場合の対応を定める 緊急連絡先、対応手順などを記載 治験開始時 治験責任医師、院内関係者と協議して作成
まとめ
CRCが作成する書類は多岐に渡りますが、いずれも治験の質と信頼性を確保するために重要な役割を果たしています。CRCは、これらの書類を正確かつ適切に作成することで、治験の円滑な進行に貢献しています。
CRCが作成する書類の例を以下にまとめます。
◆ 治験実施計画書(プロトコル)関連書類
◆ 同意説明文書
◆ 症例報告書(CRF、eCRF)
◆ 治験薬管理に関する書類
◆ モニタリング報告書
◆ 有害事象報告書
◆ 被験者対応に関する記録
◆ その他、治験に関連する各種記録
◆ 手順書・マニュアル
◆ 会議資料項目 説明 治験実施計画書関連 プロトコル概要説明資料、院内手順書 被験者関連 同意説明文書、同意書、服薬説明書、服薬日誌 症例報告書関連 症例報告書(CRF)、原資料 その他 モニタリング報告書、治験薬管理記録、緊急時対応手順書
※CRC転職に特化したAIアシスタントを利用したい方はこちらから








 年収査定はこちら
年収査定はこちら
 合格予想はこちら
合格予想はこちら
 掲示板で質問をする
掲示板で質問をする






 CRC
CRC

 CRCの
CRCの
 CRCの
CRCの
 CRCの
CRCの
 CRCの
CRCの
 CRCに
CRCに
 CRCの
CRCの
 SMO
SMO
 SMO
SMO
 応募先の
応募先の
 治験
治験
 院内CRCと
院内CRCと



 2027年4月からの転職
2027年4月からの転職 CRC未経験特集
CRC未経験特集 CRC経験者特集
CRC経験者特集 看護師特集
看護師特集 臨床検査技師特集
臨床検査技師特集 保健師特集
保健師特集 薬剤師特集
薬剤師特集 管理栄養士特集
管理栄養士特集 臨床工学技士特集
臨床工学技士特集 理学療法士特集
理学療法士特集 作業療法士特集
作業療法士特集 臨床心理士特集
臨床心理士特集 MR特集
MR特集 CRA経験者特集
CRA経験者特集


 求人検索
求人検索  ログイン
ログイン 会員さま専用
会員さま専用 CRCの仕事
CRCの仕事  治験業界の研究
治験業界の研究 経験・資格別の注意点
経験・資格別の注意点 応募書類の作成
応募書類の作成 面接・適性検査の対策
面接・適性検査の対策 みんなのクチコミ
みんなのクチコミ みんなの質問と回答
みんなの質問と回答 転職成功事例
転職成功事例 マンガで分かるCRC
マンガで分かるCRC CRCばんくチャンネル
CRCばんくチャンネル 便利な機能
便利な機能 相談/年収査定/合格予想
相談/年収査定/合格予想 2027年から働くには?
2027年から働くには? 退職手続き
退職手続き 開催中のキャンペーン
開催中のキャンペーン 《CRCばんく》とは
《CRCばんく》とは